Светает. Въедливая трель будильника медленно, но неумолимо разрушает мягкий кокон сна. Мужчина вслепую хлопает ладонью по прикроватной тумбочке. Маленький механический садист подскакивает, падает на пол и затихает с обиженным «Дзинььь». Женщина с наслаждением потягивается.
— Дорогой, пора вставать. Кофе сделай.
Мужчина, путаясь в рукавах халата, бредет на кухню. Берет турку. Аккуратно, в секретной пропорции, смешивает арабику и робусту. На кончике ножа добавляет корицу. Открывает кран. Подставляет кувшин под струю воды и вздрагивает от неожиданности. Кувшин заполнен мутной, ржавой субстанцией.
Знакомая ситуация? Если ответ — да, то эта статья для Вас!

Почему, спустя несколько минут, чистая вода приобрела столь неаппетитный вид? В чем причина такой метаморфозы?
В состав природной воды, помимо солей и минералов, входит и один из самых распространенных на Земле элементов таблицы Менделеева — железо. Есть оно и в воде, подаваемой по городским трассам водоснабжения. Всемирная организация здравоохранения (ВОЗ), установила гранично-допустимое содержание Fe в питьевой воде на уровне 0,3 мг/литр. Директива Европейского Союза № 98/83/ЕС еще «строже» — не более 0,2 мг/литр. Превышение именно этого показателя не дало нашим героям насладиться совместным утренним кофе.
Наиболее высокое содержание Fe2+ наблюдается в подземных водоемах и в воде, добытой из артезианских скважин. Причина проста — размытие и растворение железосодержащих пород, входящих в состав земной коры. Такая вода поначалу прозрачна и чиста, но, контактируя с воздухом, железо, быстро окисляется, придавая жидкости бурый цвет и выпадая на дно в виде ржавого осадка.
Вносят свою лепту и городские очистные системы, и старая, времен СССР, чугунная водотранспортная система. В результате, норма содержания железа в питьевой воде превышена в десятки раз, а из крана льется бурая, дурнопахнущая жидкость.

В чем же опасность такой воды? Во-первых, ее неприятно пить. Само по себе железо не является отравой для человеческого организма, однако представьте себе борщ, приготовленный на такой основе. Во-вторых, не опасны растворенные в воде ионы Fe2+ . А ржавые хлопья окисла железа с большой вероятностью приведут к нежелательным отложениям в почках и мочекаменной болезни. Постоянное употребление воды с высоким содержанием железа негативно сказывается и на сердечно-сосудистой системе. В третьих, не стоит забывать об аллергических реакциях организма. Кому-то душ из такой воды будет просто неприятен, а кто-то покроется сыпью и пятнами. Особенно чувствительны слизистые оболочки.
Также, вода с повышенным содержанием железа мало пригодна и для технических нужд. Постиранное с ее помощью белье приобретет «красивый», серо-буро-малиновый оттенок. Нагревательные тэны и барабан «стиралки» покроются толстым слоем рыжеватой накипи и в считанные недели выйдут из строя. Под постоянной угрозой находится и сантехническое оборудование Вашей квартиры. И если унитаз пострадает только внешне (ржавые потеки в чаше), то газовая колонка, бойлер и смесители забьются ржавчиной и выйдут из строя через каких-нибудь полгода эксплуатации.

Но железистая вода — не приговор. Если норма превышена в 3-5 раз, угрозы для бытовой техники нет, а с очисткой воды для питья и готовки справится качественный бытовой фильтр, работающий на принципе ультрафильтрации или обратного осмоса, или фильтр со специализированными картриджами, обезжелезивающими. Если же превышение исчисляется десятками раз, на помощь придет фильтр по очистке водопроводной воды от железа.
Принципы работы такого оборудования просты и понятны человеку, прослушавшему школьный курс химии. Первый шаг — перевод растворенного двухвалентного железа Fe2+ в твердое состояние путем окисления. Способ достижения — принудительная аэрация очищаемой воды. Второй шаг — отстаивание полученной смеси. Крупные фрагменты ржавчины выпадают в осадок, а частично очищенная вода подается на фильтрующие загрузки, задерживающие мельчайшую, не отстоявшуюся взвесь.
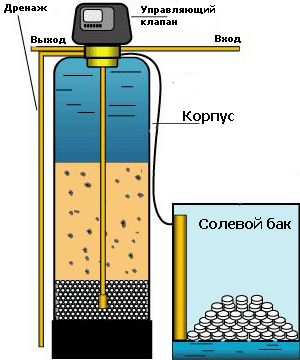
В результате на выход поступает прозрачная и вкусная вода.


